NOMENCLATURA
En
química orgánica de los alcoholes se implementa también el sistema de
nomenclatura (utilizado en cetonas y éteres también) para nombrarlos:
COMUNES
= Se
utiliza la palabra alcohol de primero a la base de alcano y simplemente se
sustituye el sufijo “ano” por “ílico”
Ej. METANO → alcohol metílico
IUPAC = Se añade una “l” al
sufijo “ano”
Ej. METANO → metanol
“Met”
→ un átomo de carbono
“Ano”
→ un hidrocarburo alcano
“L”
→ se trata de un alcohol
En
ocasiones también se hace necesario el numerar el número del compuesto en la
cadena de la molécula, dependiendo de qué tan larga sea esta
“Prefijo”
→ Cantidad de carbonos de una molécula
ÁCIDEZ DE ALCOHOLES
Los alcoholes son especies anfóteras (anfipróticas), pueden actuar como ácidos o bases. En disolución acuosa se establece un equilibrio entre el alcohol, el agua y sus bases conjugadas.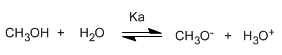
Escribiendo la constante del equilibrio (Ka)
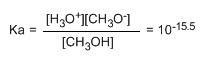
OXIDACIÓN DE ALCOHOLES
La oxidación de alcoholes forma compuestos carbonilos. Al oxidar alcoholes primarios se obtienen aldehídos, mientras que la oxidación de alcoholes secundarios forma cetonas.
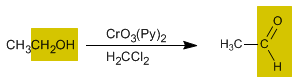
Oxidación de alcoholes primarios a aldehídos
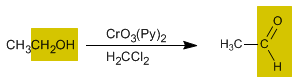
TOMADO Y ADAPTADO DE:
https://www.quimicaorganica.org/alcoholes.html
POR:
Lizeth Benítez




